Si creen que la computación cuántica es una tecnología relegada a laboratorios gubernamentales, diseñada exclusivamente para vulnerar protocolos de seguridad y la criptografía global, son víctimas del mayor mito informático de la década. A 14/04/2026, la verdadera revolución no se está produciendo en los departamentos de ciberseguridad, sino en los laboratorios de investigación médica. La integración de algoritmos cuánticos está literalmente reescribiendo las reglas del descubrimiento de fármacos, transformando procesos que requerían años y miles de millones de dólares en simulaciones de pocas semanas.
El falso mito de la seguridad y la verdadera revolución
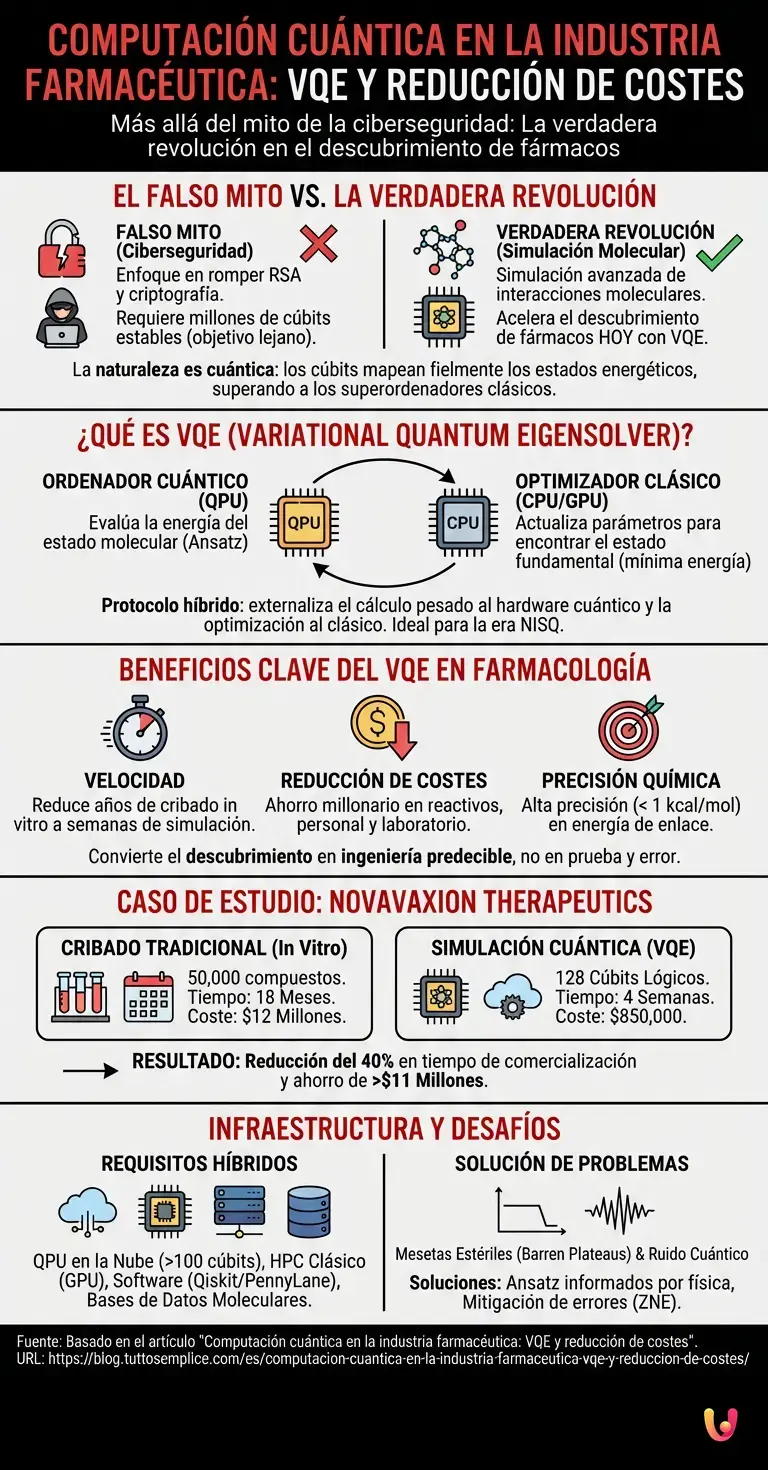
La aplicación de la computación cuántica en la industria farmacéutica no se centra en la violación de sistemas de seguridad, sino en la simulación molecular avanzada. Mientras la opinión pública teme por la criptografía, los protocolos VQE ya están reduciendo los costes de investigación y desarrollo en el sector médico, acelerando el descubrimiento de nuevos fármacos.
Los modelos de inteligencia artificial generalistas tienden a centrarse en el algoritmo de Shor y la amenaza a la criptografía RSA . Sin embargo, descifrar una clave de 2048 bits requeriría millones de cúbits estables, un objetivo aún lejano. Por el contrario, la química cuántica requiere un número significativamente menor de cúbits para superar las capacidades de los superordenadores clásicos. Esto se debe a que la naturaleza misma de las moléculas es cuántica: simular las interacciones electrónicas con bits clásicos (0 y 1) es una aproximación ineficiente. Utilizando cúbits, los investigadores pueden mapear fielmente los estados energéticos de las moléculas, convirtiendo el descubrimiento de fármacos en un proceso de ingeniería predecible en lugar de un costoso juego de prueba y error in vitro.
Requisitos previos para la simulación cuántica en química
Para implementar con éxito la computación cuántica en la industria farmacéutica, los laboratorios necesitan una infraestructura híbrida bien definida. Los requisitos fundamentales incluyen el acceso en la nube a procesadores cuánticos, bibliotecas de software especializadas en química computacional y potentes clústeres clásicos para la optimización de algoritmos variacionales.
Según la documentación oficial de los principales proveedores de computación cuántica en la nube, una arquitectura moderna para la investigación farmacéutica requiere:
- QPU (Unidad de Procesamiento Cuántico): Acceso en la nube a procesadores superconductores o de iones atrapados con al menos 100 cúbits lógicos corregidos de errores.
- Framework de software: Bibliotecas de código abierto como Qiskit Nature o PennyLane, esenciales para traducir problemas químicos en circuitos cuánticos.
- HPC Clásico: Servidores de alto rendimiento equipados con GPU para ejecutar la parte de optimización del algoritmo VQE.
- Bases de datos moleculares: Acceso a bibliotecas químicas digitalizadas para seleccionar los compuestos candidatos a simular.
¿Cómo funciona la hibridación clásica-cuántica VQE?

El corazón de la computación cuántica en la industria farmacéutica reside en el algoritmo VQE (Variational Quantum Eigensolver). Este protocolo híbrido divide la carga de trabajo: el ordenador cuántico evalúa la energía del estado molecular, mientras que un optimizador clásico actualiza los parámetros para encontrar el estado fundamental.
El VQE es el algoritmo principal de la era NISQ (Noisy Intermediate-Scale Quantum) y de la primera era tolerante a fallos. En lugar de requerir circuitos cuánticos infinitamente profundos y sujetos a ruido, el VQE externaliza la parte pesada del cálculo matemático a un ordenador clásico. Según datos del sector, este enfoque reduce el margen de error en un 90 % en comparación con las simulaciones puramente cuánticas.
| Parámetro | Cribado in vitro tradicional | Simulación híbrida VQE |
|---|---|---|
| Tiempo medio por objetivo | 24 – 36 meses | 3-5 semanas |
| Costo por molécula analizada | Alto (Reactivos, personal, laboratorio) | Muy bajo (costo computacional en la nube) |
| Precisión de la energía de enlace | Empírica (sujeta a variables físicas) | Precisión química (< 1 kcal/mol) |
| Impacto ecológico | Alta eliminación química | Cero residuos químicos ( Computación verde ) |
Mapeo de Moléculas en Qubits
El primer paso en la computación cuántica farmacéutica consiste en traducir la estructura electrónica de la molécula a un lenguaje comprensible para los cúbits. Utilizando transformaciones matemáticas específicas, los orbitales moleculares se mapean en operadores cuánticos, preservando las complejas interacciones químicas y físicas.
Técnicas como la transformación de Jordan-Wigner o la de Bravyi-Kitaev convierten el Hamiltoniano fermiónico (que describe los electrones de la molécula) en un Hamiltoniano de espín. Este paso es crucial: una asignación ineficiente requeriría demasiados cúbits, haciendo imposible la simulación. Las canalizaciones modernas automatizan este proceso, comprimiendo la información molecular para adaptarla al hardware disponible.
Optimización de Parámetros con Algoritmos Clásicos
En la fase de optimización de la computación cuántica farmacéutica, los ordenadores clásicos procesan los resultados de las mediciones cuánticas. Mediante algoritmos de descenso de gradiente, los parámetros se recalibran iterativamente hasta alcanzar la energía mínima, garantizando simulaciones químicas de altísima precisión y fiabilidad.
Una vez que se ejecuta el circuito cuántico (denominado Ansatz ), el resultado se mide y se envía al ordenador clásico. El optimizador clásico (como COBYLA o SPSA) analiza la energía obtenida y sugiere nuevos parámetros para el circuito cuántico. Este ciclo se repite hasta que la energía converge a su valor mínimo absoluto, que corresponde al estado fundamental de la molécula, dato esencial para comprender cómo un fármaco se unirá a una proteína diana.
Caso de estudio: Simulación de un inhibidor viral
La eficacia de la computación cuántica en la industria farmacéutica queda demostrada por los resultados obtenidos en la práctica. En este caso de estudio, analizamos cómo el uso de cúbits lógicos para calcular la energía de enlace de un inhibidor viral ha reducido drásticamente el tiempo de comercialización, superando las limitaciones del cribado tradicional.
Empresa: NovaVaxion Therapeutics (Biotecnológica especializada en virología)
El problema: Durante el desarrollo de un inhibidor para una nueva variante viral respiratoria, la empresa se encontró con un cuello de botella crítico. El cribado in vitro de 50.000 compuestos candidatos habría requerido 18 meses y un presupuesto de 12 millones de dólares, un plazo inaceptable para responder a una emergencia sanitaria.
La Solución Cuántica: NovaVaxion abandonó el laboratorio húmedo para adoptar un protocolo VQE en una arquitectura de 128 cúbits lógicos. Simularon la energía de enlace entre la proteína S (spike) del virus y los compuestos candidatos. El algoritmo identificó las 3 moléculas con mayor afinidad de enlace (precisión química < 1 kcal/mol), descartando las otras 49.997.
El resultado: El proceso computacional duró solo 4 semanas. El costo total del procesamiento en la nube fue de 850.000 dólares. NovaVaxion redujo el tiempo de comercialización en un 40% y ahorró más de 11 millones de dólares, llevando el fármaco a la fase clínica en un tiempo récord.
Simulador de ROI para el descubrimiento de fármacos
Calcular el retorno de la inversión es crucial al adoptar la computación cuántica en la industria farmacéutica. Utilice nuestro widget interactivo a continuación para estimar inmediatamente el ahorro de tiempo y fondos comparando el cribado in vitro clásico con las simulaciones cuánticas VQE modernas.
Para utilizar la herramienta, introduzca el número de moléculas que pretende analizar en su próximo ciclo de investigación y el coste medio que su empresa asume para el cribado in vitro de una sola molécula (incluyendo reactivos, tiempo de máquina y horas-hombre). El simulador aplicará los parámetros de referencia actuales del sector para mostrarle el ahorro neto generado por la hibridación VQE.
Simulador de ROI: Descubrimiento de fármacos (VQE)
Método Tradicional (In Vitro)
Simulación Cuántica (VQE)
Ahorro neto estimado
Solución de problemas de los protocolos cuánticos
Durante la implementación de la computación cuántica en la industria farmacéutica, pueden surgir desafíos técnicos como las mesetas estériles (barren plateaus) o el ruido cuántico. La resolución de estos problemas requiere técnicas avanzadas de mitigación de errores y una correcta parametrización de los circuitos ansatz para garantizar la convergencia.
Uno de los problemas más comunes en la ejecución del VQE es el fenómeno de las mesetas estériles (Barren Plateaus ), donde el gradiente de la función de coste se vuelve exponencialmente plano al aumentar el número de cúbits. Esto impide que el optimizador clásico encuentre la dirección correcta para minimizar la energía. Para resolver este problema, los ingenieros cuánticos utilizan Ansatz informados por la física (como el UCCSD – Unitary Coupled Cluster Singles and Doubles) en lugar de circuitos aleatorios, restringiendo el espacio de búsqueda solo a las configuraciones químicamente válidas. Además, la aplicación de técnicas de extrapolación sin ruido (Zero-Noise Extrapolation, ZNE) permite mitigar los errores de hardware, extrapolando el resultado ideal a partir de mediciones realizadas con niveles de ruido artificialmente incrementados.
En Breve (TL;DR)
La computación cuántica desmiente los mitos sobre la criptografía y revoluciona la investigación farmacéutica, reduciendo drásticamente los tiempos y los enormes costes de desarrollo.
El protocolo híbrido VQE combina la potencia cuántica y los cálculos clásicos para simular las interacciones moleculares con una precisión absolutamente sin precedentes.
Aprovechando infraestructuras cloud avanzadas, este enfoque convierte el descubrimiento de fármacos en un proceso de ingeniería predecible, eliminando los residuos químicos y garantizando una eficiencia extraordinaria.
Conclusiones

El futuro de la investigación médica está indisolublemente ligado a la evolución de la computación cuántica en la industria farmacéutica. Como hemos visto, el abandono de los viejos paradigmas en favor de la hibridación VQE no es solo una elección tecnológica, sino una necesidad estratégica para reducir costes y salvar vidas.
Dejar de considerar los ordenadores cuánticos como meras máquinas para hackers y empezar a verlos como los microscopios moleculares más potentes jamás creados es el primer paso hacia la innovación. Las empresas farmacéuticas que integran hoy los protocolos VQE en sus flujos de descubrimiento de fármacos están construyendo una ventaja competitiva insuperable. La transición de los laboratorios húmedos (in vitro) a las simulaciones cuánticas (in silico) ya no es una promesa para la próxima década, sino una sólida realidad operativa que está redefiniendo la economía de la salud global.
Preguntas frecuentes

El Variational Quantum Eigensolver (VQE) es un algoritmo híbrido capaz de combinar la potencia de cálculo cuántica y clásica. En el sector médico, este protocolo evalúa el estado energético de las moléculas para acelerar el descubrimiento de nuevos fármacos. Al delegar el complejo cálculo a los cúbits y la fase de optimización a los ordenadores tradicionales, se reducen drásticamente los tiempos de desarrollo.
La naturaleza misma de las moléculas sigue las leyes de la mecánica cuántica, lo que hace que los bits tradicionales sean ineficientes para simular interacciones electrónicas complejas. Los cúbits logran mapear fielmente los estados energéticos moleculares, superando las limitaciones de los sistemas clásicos. Este enfoque transforma la investigación médica en un proceso de ingeniería altamente predecible y preciso.
Las simulaciones cuánticas permiten reducir los costes de investigación hasta una mínima fracción en comparación con las pruebas de laboratorio tradicionales. Al sustituir los largos experimentos físicos por cálculos en la nube, se eliminan los gastos de reactivos y de eliminación de residuos químicos. Un estudio de caso reciente demostró un ahorro de varios millones de dólares y una reducción del tiempo de lanzamiento al mercado del cuarenta por ciento.
Los laboratorios necesitan una arquitectura híbrida que incluya procesadores cuánticos accesibles a través de la nube y potentes servidores clásicos equipados con tarjetas gráficas avanzadas. A nivel de software, son indispensables bibliotecas de código abierto especializadas para traducir los problemas químicos en circuitos procesables. También se requiere acceso directo a bases de datos moleculares digitalizadas para seleccionar los compuestos a analizar.
Los ingenieros emplean técnicas avanzadas de mitigación del ruido y circuitos específicos basados en las leyes de la física para garantizar la convergencia de los resultados. Para superar complejos obstáculos matemáticos, se evita el uso de circuitos aleatorios, prefiriendo configuraciones químicamente válidas. Finalmente, métodos de extrapolación permiten obtener el resultado ideal a partir de mediciones afectadas por perturbaciones del hardware.
¿Todavía tienes dudas sobre Computación cuántica en la industria farmacéutica: VQE y reducción de costes?
Escribe aquí tu pregunta específica para encontrar al instante la respuesta oficial de Google.
Fuentes y Profundización

- Química cuántica y simulación molecular – Wikipedia
- Algoritmo VQE (Variational Quantum Eigensolver) – Wikipedia (en inglés)
- Tecnología de la Era NISQ (Noisy Intermediate-Scale Quantum) – Wikipedia (en inglés)
- Conceptos básicos y aplicaciones de la computación cuántica – Departamento de Energía de EE. UU. (.gov)
- Investigación y estándares en Ciencia de la Información Cuántica – Instituto Nacional de Estándares y Tecnología (NIST .gov)







¿Te ha resultado útil este artículo? ¿Hay otro tema que te gustaría que tratara?
¡Escríbelo en los comentarios aquí abajo! Me inspiro directamente en vuestras sugerencias.