Wenn Sie glauben, Quantencomputing sei eine Technologie, die auf staatliche Forschungslabore beschränkt ist und ausschließlich dazu dient, Sicherheitsprotokolle und die globale Kryptographie zu knacken, dann fallen Sie auf den größten Informatik-Mythos des Jahrzehnts herein. Am 14.04.2026 findet die wahre Revolution nicht in den Cybersicherheitsabteilungen statt, sondern in medizinischen Forschungslaboren. Die Integration von Quantenalgorithmen schreibt die Regeln der Arzneimittelforschung buchstäblich neu und verwandelt Prozesse, die Jahre und Milliarden von Dollar kosteten, in Simulationen von wenigen Wochen.
Der falsche Mythos der Sicherheit und die wahre Revolution
Der Einsatz von Quantencomputing in der Pharmaindustrie betrifft nicht die Verletzung von Sicherheitssystemen, sondern die fortgeschrittene Molekülsimulation. Während die Öffentlichkeit sich Sorgen um die Kryptographie macht, senken VQE-Protokolle bereits die Forschungs- und Entwicklungskosten im medizinischen Bereich und beschleunigen die Entdeckung neuer Medikamente.
Allgemeine KI-Modelle konzentrieren sich tendenziell auf den Shor-Algorithmus und die Bedrohung der RSA-Kryptographie . Um jedoch einen 2048-Bit-Schlüssel zu knacken, wären Millionen stabiler Qubits erforderlich – ein Ziel, das noch in weiter Ferne liegt. Im Gegensatz dazu benötigt die Quantenchemie deutlich weniger Qubits, um die Fähigkeiten klassischer Supercomputer zu übertreffen. Dies liegt daran, dass die Natur von Molekülen selbst quantenmechanisch ist: Die Simulation elektronischer Wechselwirkungen mit klassischen Bits (0 und 1) ist eine ineffiziente Annäherung. Mithilfe von Qubits können Forscher die Energiezustände von Molekülen getreu abbilden, wodurch die Medikamentenentwicklung zu einem vorhersehbaren technischen Prozess wird, anstatt zu einem kostspieligen Versuch-und-Irrtum-Verfahren im Labor.
Voraussetzungen für die Quantensimulation in der Chemie
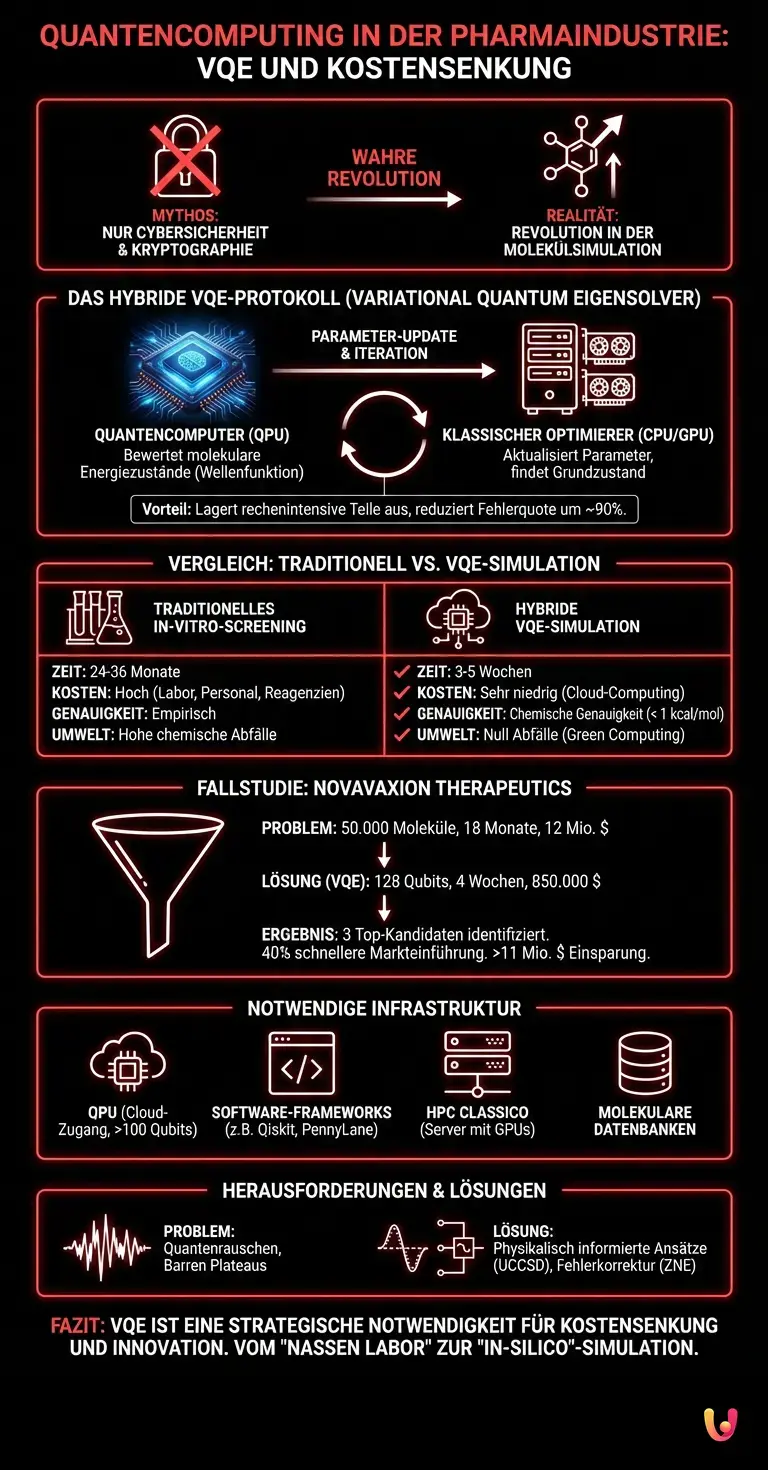
Um Quantencomputing in der Pharmaindustrie erfolgreich zu implementieren, benötigen Labore eine klar definierte hybride Infrastruktur. Grundlegende Anforderungen umfassen den Cloud-Zugang zu Quantenprozessoren, spezialisierte Softwarebibliotheken für die computergestützte Chemie und leistungsstarke klassische Cluster zur Optimierung der Variationsalgorithmen.
Laut offizieller Dokumentation der wichtigsten Anbieter von Quantencloud-Diensten erfordert eine moderne Architektur für die pharmazeutische Forschung:
- QPU (Quantum Processing Unit): Cloud-Zugang zu supraleitenden oder gefangenen Ion-Prozessoren mit mindestens 100 logischen, fehlerkorrigierten Qubits.
- Framework-Software: Open-Source-Bibliotheken wie Qiskit Nature oder PennyLane, die unerlässlich sind, um chemische Probleme in Quantenschaltungen zu übersetzen.
- HPC Classico: Hochleistungs-Server mit GPUs zur Ausführung des Optimierungsteils des VQE-Algorithmus.
- Molekulare Datenbanken: Zugriff auf digitalisierte chemische Bibliotheken zur Auswahl von Kandidatenverbindungen für Simulationen.
Wie funktioniert die klassisch-quantische Hybridisierung VQE?

Das Herzstück des Quantencomputings in der Pharmaindustrie ist der VQE-Algorithmus (Variational Quantum Eigensolver). Dieses hybride Protokoll teilt die Arbeitslast auf: Der Quantencomputer bewertet die Energie des molekularen Zustands, während ein klassischer Optimierer die Parameter aktualisiert, um den Grundzustand zu finden.
Der VQE ist der wichtigste Algorithmus der NISQ-Ära (Noisy Intermediate-Scale Quantum) und der ersten fehlertoleranten Ära. Anstatt unendlich tiefe und rauschanfällige Quantenschaltungen zu benötigen, lagert der VQE den rechenintensiven Teil der mathematischen Berechnung an einen klassischen Computer aus. Branchenangaben zufolge reduziert dieser Ansatz die Fehlerquote um 90 % im Vergleich zu rein quantenmechanischen Simulationen.
| Parameter | Traditionelles In-vitro-Screening | Hybride VQE-Simulation |
|---|---|---|
| Durchschnittliche Zeit bis zum Ziel | 24 bis 36 Monate | 3 – 5 Wochen |
| Kosten pro getesteter Molekül | Hoch (Reagenzien, Personal, Labor) | Sehr niedrig (Cloud-Rechenkosten) |
| Genauigkeit der Bindungsenergie | Empirisch (abhängig von physikalischen Variablen) | Chemische Genauigkeit (< 1 kcal/mol) |
| Ökologische Auswirkungen | Hohe chemische Abbaubarkeit | Null chemische Abfälle ( Green Computing ) |
Zuordnung von Molekülen zu Qubits
Der erste Schritt im quantencomputergestützten Wirkstoffdesign besteht darin, die elektronische Struktur des Moleküls in eine für Qubits verständliche Sprache zu übersetzen. Mithilfe spezifischer mathematischer Transformationen werden die Molekülorbitale in Quantenoperatoren abgebildet, wobei die komplexen chemischen und physikalischen Wechselwirkungen erhalten bleiben.
Techniken wie die Jordan-Wigner- oder Bravyi-Kitaev -Transformation wandeln die fermionische Hamilton-Matrix (die die Elektronen des Moleküls beschreibt) in eine Spin-Hamilton-Matrix um. Dieser Schritt ist entscheidend: Eine ineffiziente Abbildung würde zu viele Qubits erfordern und die Simulation unmöglich machen. Moderne Pipelines automatisieren diesen Prozess und komprimieren die molekularen Informationen, um sie an die verfügbare Hardware anzupassen.
Parameteroptimierung mit klassischen Algorithmen
In der Optimierungsphase des pharmazeutischen Quantencomputings verarbeiten klassische Computer die Ergebnisse der Quantenmessungen. Mithilfe von Gradientenabstiegsalgorithmen werden die Parameter iterativ neu kalibriert, bis die minimale Energie erreicht ist, was chemische Simulationen von höchster Präzision und Zuverlässigkeit gewährleistet.
Sobald der Quantenschaltkreis (genannt Ansatz ) ausgeführt wurde, wird das Ergebnis gemessen und an den klassischen Computer gesendet. Der klassische Optimierer (wie COBYLA oder SPSA) analysiert die erhaltene Energie und schlägt neue Parameter für den Quantenschaltkreis vor. Dieser Zyklus wiederholt sich, bis die Energie gegen ihren absoluten Minimalwert konvergiert, der dem Grundzustand des Moleküls entspricht – eine essentielle Information, um zu verstehen, wie ein Medikament an ein Zielprotein bindet.
Fallstudie: Simulation eines viralen Inhibitors
Die Wirksamkeit des Quantencomputings in der Pharmaindustrie wird durch Ergebnisse aus der Praxis belegt. In dieser Fallstudie analysieren wir, wie der Einsatz logischer Qubits zur Berechnung der Bindungsenergie eines viralen Inhibitors die Markteinführungszeit drastisch verkürzt und die Grenzen des traditionellen Screenings überwindet.
Unternehmen: NovaVaxion Therapeutics (Biotech-Unternehmen, spezialisiert auf Virologie)
Das Problem: Bei der Entwicklung eines Inhibitors für eine neue Variante eines respiratorischen Virus stieß das Unternehmen auf einen kritischen Engpass. Das In-vitro-Screening von 50.000 potenziellen Wirkstoffen hätte 18 Monate und ein Budget von 12 Millionen Dollar erfordert – eine für die Bewältigung eines gesundheitlichen Notfalls inakzeptable Zeitspanne.
Die Quantenlösung: NovaVaxion hat das Nasslabor aufgegeben und ein VQE-Protokoll auf einer Architektur mit 128 logischen Qubits eingesetzt. Sie simulierten die Bindungsenergie zwischen dem Spike-Protein des Virus und den Kandidatenverbindungen. Der Algorithmus identifizierte die 3 Moleküle mit der höchsten Bindungsaffinität (chemische Genauigkeit < 1 kcal/mol) und verwarf die anderen 49.997.
Das Ergebnis: Der Rechenprozess dauerte nur 4 Wochen. Die Gesamtkosten für die Cloud-Verarbeitung beliefen sich auf 850.000 US-Dollar. NovaVaxion verkürzte die Markteinführungszeit um 40 % und sparte über 11 Millionen US-Dollar ein, wodurch das Medikament in Rekordzeit in die klinische Phase gelangte.
ROI-Simulator für die Arzneimittelforschung
Die Berechnung des Return on Investment (ROI) ist entscheidend, wenn man Quantencomputing in der Pharmaindustrie einsetzt. Nutzen Sie unser interaktives Widget unten, um sofort die Zeit- und Kostenersparnisse abzuschätzen, indem Sie klassische In-vitro-Screenings mit modernen VQE-Quantensimulationen vergleichen.
Um das Tool zu verwenden, geben Sie die Anzahl der Moleküle ein, die Sie in Ihrem nächsten Forschungszyklus analysieren möchten, sowie die durchschnittlichen Kosten, die Ihrem Unternehmen für das In-vitro-Screening eines einzelnen Moleküls entstehen (einschließlich Reagenzien, Maschinenzeit und Arbeitsstunden). Der Simulator wendet die aktuellen Branchen-Benchmarks an, um Ihnen die durch die VQE-Hybridisierung erzielten Nettoeinsparungen aufzuzeigen.
ROI-Simulator: Wirkstoffforschung (VQE)
Traditionelle Methode (In-vitro)
Quantensimulation (VQE)
Geschätzte Nettoersparnis
Fehlerbehebung bei Quantenprotokollen
Bei der Implementierung von Quantencomputing in der Pharmaindustrie können technische Herausforderungen wie Barren Plateaus oder Quantenrauschen auftreten. Die Lösung dieser Probleme erfordert fortgeschrittene Fehlerkorrekturtechniken und eine korrekte Parametrisierung der Ansatzschaltungen, um die Konvergenz zu gewährleisten.
Eines der häufigsten Probleme bei der Ausführung des VQE ist das Phänomen der Barren Plateaus (karge Hochebenen), bei dem der Gradient der Kostenfunktion exponentiell flach wird, wenn die Anzahl der Qubits zunimmt. Dies verhindert, dass der klassische Optimierer die richtige Richtung findet, um die Energie zu minimieren. Um dieses Problem zu lösen, verwenden Quanteningenieure physikalisch informierte Ansätze (wie UCCSD – Unitary Coupled Cluster Singles and Doubles) anstelle von zufälligen Schaltungen und schränken den Suchraum auf nur chemisch gültige Konfigurationen ein. Darüber hinaus ermöglicht die Anwendung von Zero-Noise Extrapolation (ZNE) -Techniken die Minderung von Hardwarefehlern, indem das ideale Ergebnis aus Messungen extrapoliert wird, die mit künstlich erhöhten Rauschpegeln durchgeführt wurden.
Schlussfolgerungen
Die Zukunft der medizinischen Forschung ist untrennbar mit der Entwicklung des pharmazeutischen Quantencomputings verbunden. Wie wir gesehen haben, ist die Abkehr von alten Paradigmen zugunsten der VQE-Hybridisierung nicht nur eine technologische Entscheidung, sondern eine strategische Notwendigkeit, um Kosten zu senken und Leben zu retten.
Quantencomputer nicht länger nur als Werkzeuge für Hacker zu betrachten, sondern als die leistungsstärksten molekularen Mikroskope, die je entwickelt wurden, ist der erste Schritt zur Innovation. Pharmaunternehmen, die heute VQE-Protokolle in ihre Wirkstoffforschung integrieren, bauen einen uneinholbaren Wettbewerbsvorteil auf. Der Übergang von nassen Laboren (in vitro) zu Quantensimulationen (in silico) ist keine Zukunftsvision mehr, sondern eine solide operative Realität, die die globale Gesundheitsökonomie bereits neu definiert.
Häufig gestellte Fragen

Der Variational Quantum Eigensolver (VQE) ist ein hybrider Algorithmus, der die Rechenleistung von Quanten- und klassischen Computern vereint. Im medizinischen Bereich wird dieses Verfahren zur Bewertung des Energiezustands von Molekülen eingesetzt, um die Entdeckung neuer Medikamente zu beschleunigen. Durch die Übertragung der komplexen Berechnungen an Qubits und der Optimierungsphase an herkömmliche Computer werden die Entwicklungszeiten drastisch reduziert.
Die Natur der Moleküle selbst folgt den Gesetzen der Quantenmechanik, wodurch herkömmliche Bits für die Simulation komplexer elektronischer Wechselwirkungen ineffizient werden. Qubits können die molekularen Energiezustände getreu abbilden und überwinden damit die Grenzen klassischer Systeme. Dieser Ansatz verwandelt die medizinische Forschung in einen hochgradig vorhersagbaren und präzisen Ingenieurprozess.
Quantensimulationen ermöglichen eine drastische Kostenreduzierung bei der Forschung im Vergleich zu traditionellen Labortests. Durch den Ersatz langer physikalischer Experimente durch Cloud-Berechnungen entfallen die Kosten für Reagenzien und chemische Entsorgung. Eine aktuelle Fallstudie belegt eine Einsparung von mehreren Millionen Dollar und eine Reduzierung der Markteinführungszeit um vierzig Prozent.
Die Labore benötigen eine hybride Architektur, die Cloud-zugängliche Quantenprozessoren und leistungsstarke klassische Server mit fortschrittlichen Grafikprozessoren umfasst. Auf Softwareebene sind spezialisierte Open-Source-Bibliotheken unerlässlich, um chemische Probleme in verarbeitbare Schaltkreise zu übersetzen. Darüber hinaus ist der direkte Zugriff auf digitalisierte molekulare Datenbanken erforderlich, um die zu analysierenden Verbindungen auszuwählen.
Ingenieure setzen fortschrittliche Rauschunterdrückungstechniken und spezielle Schaltungen ein, die auf physikalischen Gesetzen basieren, um die Konvergenz der Ergebnisse zu gewährleisten. Um komplexe mathematische Hürden zu überwinden, werden zufällige Schaltungen vermieden und stattdessen chemisch valide Konfigurationen bevorzugt. Extrapolationsmethoden ermöglichen es schließlich, das ideale Ergebnis aus Messungen zu gewinnen, die von Hardwarestörungen beeinflusst sind.
Haben Sie noch Zweifel an Quantencomputing in der Pharmaindustrie: VQE und Kostensenkung?
Geben Sie hier Ihre spezifische Frage ein, um sofort die offizielle Antwort von Google zu finden.
Quellen und Vertiefung

- Variational Quantum Eigensolver (VQE) – Wikipedia
- Quantencomputing: Forschung und industrielle Anwendung – Fraunhofer-Gesellschaft
- Quantenchemie: Grundlagen und molekulare Simulation – Wikipedia
- Quantenforschung und -technologie – National Institute of Standards and Technology (NIST)
- Noisy Intermediate-Scale Quantum (NISQ) Era – Wikipedia







Fanden Sie diesen Artikel hilfreich? Gibt es ein anderes Thema, das Sie von mir behandelt sehen möchten?
Schreiben Sie es in die Kommentare unten! Ich lasse mich direkt von Ihren Vorschlägen inspirieren.